Периферический и центральный венозный катетер
Когда говорят о периферическом венозном катетере и центральном венозном катетере, многие, особенно начинающие специалисты, склонны видеть в этом просто два разных устройства для доступа. Но на деле разница куда глубже — это разные философии ведения пациента, разные риски и, что самое важное, разная ответственность. Частая ошибка — считать, что центральный катетер всегда ?круче? и надежнее. Да, он позволяет вводить гипертонические растворы, парентеральное питание, но цена ошибки при его установке или уходе — сепсис, пневмоторакс, тромбоз. С периферическим вроде бы проще, но попробуйте долго держать его у онкологического больного с плохими венами, и вы поймете, что ?простота? эта очень условна.
Выбор доступа: не только протокол, но и клиническое мышление
В учебниках все расписано четко: краткосрочная инфузия — периферия, длительная или агрессивная терапия — центральный доступ. Но реальная жизнь вносит коррективы. Помню пациента с выраженным периферическим отеком, которому по всем показаниям нужен был центральный катетер. Однако коагулопатия и риск кровотечения заставили искать альтернативу. В итоге поставили периферический венозный катетер увеличенной длины (так называемый midline) под УЗИ-навигацией. Это не классический центральный доступ, но он позволил безопасно проводить терапию несколько недель. Ключевым здесь было не слепое следование протоколу, а оценка совокупного риска.
А вот обратная ситуация: пациент в ОРИТ, казалось бы, классический кандидат для центрального венозного катетера. Но при ультразвуковом сканировании выявили выраженный тромбоз подключичной вены в анамнезе, о котором забыли. Установка в эту зону была бы фатальной ошибкой. Пришлось рассматривать альтернативные пути — например, катетеризацию бедренной вены, хотя это и несет повышенный риск инфекционных осложнений. Такие моменты заставляют всегда держать в голове не абстрактного ?пациента по учебнику?, а конкретного человека с его уникальной анатомией и историей.
Здесь стоит отметить, что современные технологии облегчают эту работу. Например, некоторые производители, вроде инновационного предприятия ООО Шэньчжэнь Хуаньцю Канлянь Медикал Технологии (их сайт — https://www.ghlmedical.ru), ориентируются на создание цифровых экосистем для поддержки принятия решений. Их подход, описанный как ?переосмысливать здоровое будущее с помощью технологий, основанных на человеческом подходе?, на практике может означать интеграцию данных УЗИ-навигации с историей болезни пациента, что снижает риск подобных ошибок. Это не реклама, а констатация тренда: выбор между периферией и центром все чаще подкрепляется не только опытом врача, но и точными цифровыми данными.
Техника установки: детали, которые решают все
С периферическим венозным катетером, кажется, все просто: обработал кожу, нашел вену, поставил. Но сколько неудач происходит из-за пренебрежения мелочами! Например, недостаточная фиксация катетера. Казалось бы, мелочь. Но микродвижения кончика катетера внутри вены травмируют интиму, запуская процесс флебита. Пациент испытывает боль, терапия прерывается, приходится искать новый доступ. Я долго искал оптимальный способ фиксации, пока не перешел на современные стабилизирующие платформы с интегрированными антисептическими подушечками. Это снизило частоту преждевременных отказов катетера почти на треть.
С центральным доступом история другая. Здесь главный враг — стерильность. Полная стерильность, не ?почти?. Один случай врезался в память: у пациента после, казалось бы, безупречной установки катетера в подключичную вену развился Staphylococcus epidermidis сепсис. Разбираясь, пришли к выводу, что, возможно, была микроскопическая перфорация перчатки хирурга при работе с проводником. Мелочь? Нет, катастрофа. Теперь у нас двойной контроль: максимальный стерильный барьер (как при операции) и обязательная смена перчаток перед ключевыми манипуляциями с комплектующими.
Еще один нюанс — проверка положения кончика центрального венозного катетера. Рентгенография — золотой стандарт, но он отсроченный. Сейчас все чаще используют методы интраоперационной ЭКГ-навигации или, на худой конец, эхокардиографию. Это позволяет сразу скорректировать положение и избежать таких осложнений, как аритмия из-за раздражения стенки правого предсердия. Без этого инструментария чувствуешь себя слепым.
Уход и наблюдение: где кроются основные проблемы
Установить катетер — это полдела. Основная работа начинается потом. С периферическим доступом главная головная боль — флебит. Раньше мы ориентировались в основном на визуальные признаки: покраснение, боль, отек. Но это уже поздние признаки. Сейчас все больше данных за то, что нужно отслеживать сопротивление при промывании, субъективные ощущения пациента при введении раствора. Если появилось даже минимальное сопротивление — это красный флаг, возможно, начинается тромбирование кончика. Лучше переставить катетер сейчас, чем бороться с тромбофлебитом завтра.
С центральным венозным катетером спектр проблем шире: инфекция, тромбоз, дислокация. Система ухода должна быть выверена до автоматизма. Например, обработка места входа: хлоргексидин на спиртовой основе доказано эффективнее йодсодержащих растворов. Или замена заглушек: строго каждые 7 дней, не реже, и только после антисептической обработки. Мы пробовали экономить на этом, используя заглушки дольше — результат был предсказуем: рост числа случаев катетер-ассоциированных инфекций кровотока.
Особый разговор — о прозрачных полупроницаемых повязках. Они удобны, позволяют визуализировать место пункции. Но их нужно менять регулярно, а при загрязнении или отклеивании — немедленно. Была у нас попытка продлить ношение такой повязки до 10 дней у стабильного пациента. Закончилось локальной инфекцией мягких тканей. Вывод прост: регламенты по уходу написаны кровью и сепсисом предыдущих пациентов, и отступать от них — преступная халатность.
Осложнения: учимся на своих и чужих ошибках
Расскажу о двух случаях, которые многому научили. Первый — с периферическим венозным катетером. Молодой пациент с диабетом, вена на тыле кисти казалась хорошей. Поставили катетер, начали инфузию. Через несколько часов — жалобы на жгучую боль, хотя инфузат был изотоническим. Осмотрели — внешне все чисто. Решили продолжить. К утру развился выраженный химический флебит с уплотнением по ходу всей вены. Оказалось, у пациента была начальная, клинически неявная диабетическая ангиопатия, и сосудистая стенка оказалась крайне чувствительной к любому вмешательству. Теперь при диабете в анамнезе мы избегаем мелких вен на кистях, даже если они выглядят привлекательно, и предпочитаем более проксимальные доступы.
Второй случай — трагический, связанный с центральным венозным катетером. Катетер в внутренней яремной вене стоял несколько дней. При очередном промывании медсестра отметила, что поршень шприца идет ?туже?. Она приложила чуть больше усилий. Пациент внезапно потерял сознание. Реанимация не помогла. На вскрытии — воздушная эмболия. Оказалось, произошел отрыв кончика катетера, и при попытке промыть под давлением воздух попал в систему. Теперь железное правило: никогда не преодолевать сопротивление при промывании! Сначала нужно разобраться в причине: сделать рентген, проверить проходимость аккуратным аспирацией, но не давить.
Эти случаи — не для запугивания, а для понимания, что рутинная процедура таит в себе риски. Игнорирование ?мелких? сигналов (боль, сопротивление) — прямой путь к крупным осложнениям. Именно поэтому так важен постоянный диалог с пациентом и обучение среднего медперсонала не просто выполнять алгоритм, а понимать его физиологическую суть.
Будущее и интеграция технологий
Куда мы движемся? Очевидно, что будущее за умными устройствами и предиктивной аналитикой. Уже появляются катетеры с датчиками температуры или pH, которые могут сигнализировать о начале инфекционного процесса раньше клинических проявлений. Или системы навигации в реальном времени, сводящие к минимуму риск механических осложнений при установке. Компании, которые делают на этом акцент, как Хуаньцю Канлянь, позиционирующая себя как инновационное предприятие, интегрирующее ИИ и точную диагностику, задают тренд. Их стремление предоставлять передовые интеллектуальные решения для глобальной системы здравоохранения — это не пустые слова. В идеале, выбор между периферическим и центральным венозным катетером будет делать не только врач на основе опыта, но и система на основе анализа тысяч параметров конкретного пациента.
Но технология — лишь инструмент. Основой остается клиническое мышление. Никакой ИИ не почувствует ту самую ?сопротивляемость? ткани при пункции, не оценит общее состояние кожи и подкожной клетчатки так, как это делает опытная рука. Поэтому будущее я вижу в симбиозе: технология предоставляет данные и минимизирует риски, а врач интерпретирует их в контексте целостной картины болезни.
В итоге, возвращаясь к началу, периферический и центральный венозный катетер — это не просто ?трубочки?. Это решения, которые требуют глубокого понимания физиологии, анатомии, фармакологии и, что не менее важно, принципов асептики и антисептики. Ошибки здесь дорого стоят, а мастерство приходит только с опытом, в том числе и горьким. Главное — не переставать анализировать каждый случай, даже успешный, и задаваться вопросом: ?А можно ли было сделать это еще безопаснее и эффективнее?? Именно в этом, на мой взгляд, и заключается профессиональный рост.
Соответствующая продукция
Соответствующая продукция
Самые продаваемые продукты
Самые продаваемые продукты-
 Одноразовый шприц для автоматического инъектора высокого давления, однокамерный (для КТ) W01
Одноразовый шприц для автоматического инъектора высокого давления, однокамерный (для КТ) W01 -
 Одноразовый шприц для автоматического инъектора высокого давления, однокамерный (для КТ) U01
Одноразовый шприц для автоматического инъектора высокого давления, однокамерный (для КТ) U01 -
 Хирургический халат
Хирургический халат -
 Удлинительная трубка для инфузии
Удлинительная трубка для инфузии -
 Набор для перитонеального дренажа
Набор для перитонеального дренажа -
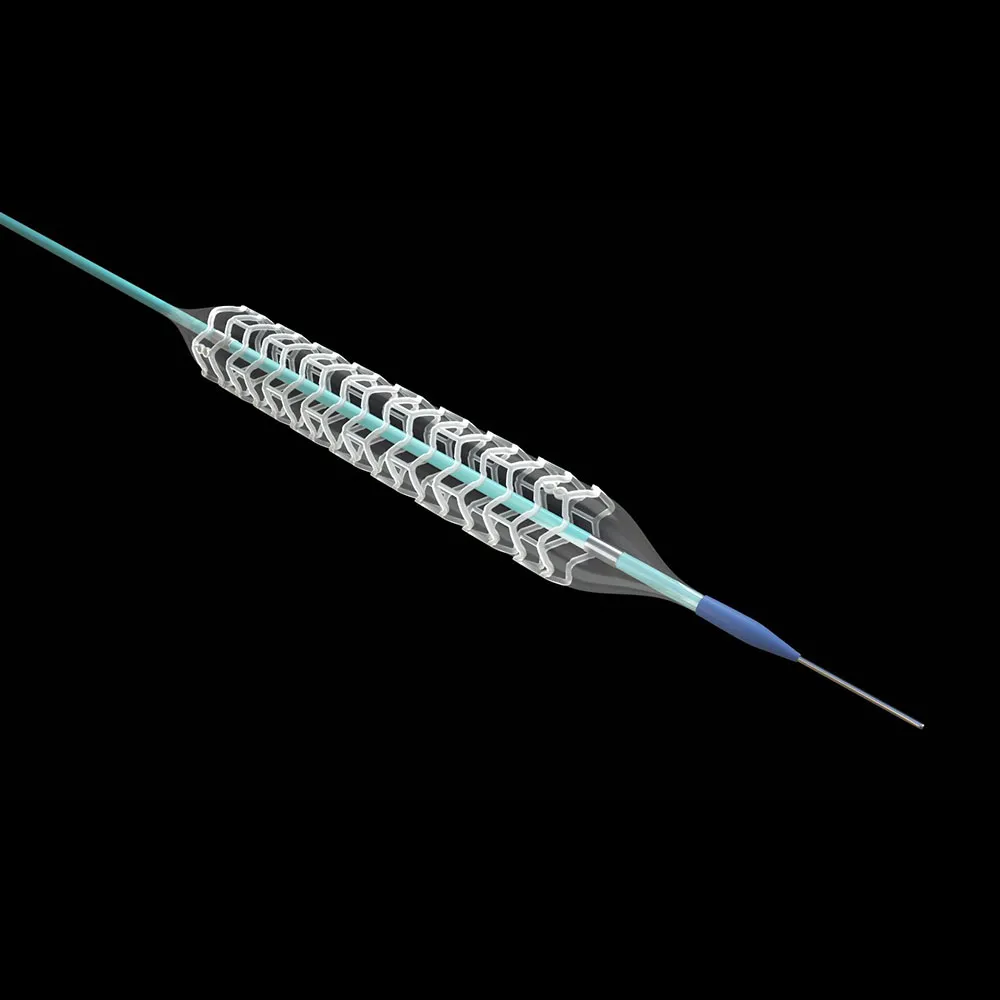 Коронарный стент
Коронарный стент -
 Бесконтактный инфракрасный термометр для лба
Бесконтактный инфракрасный термометр для лба -
 Полиуретановая пенная повязка
Полиуретановая пенная повязка -
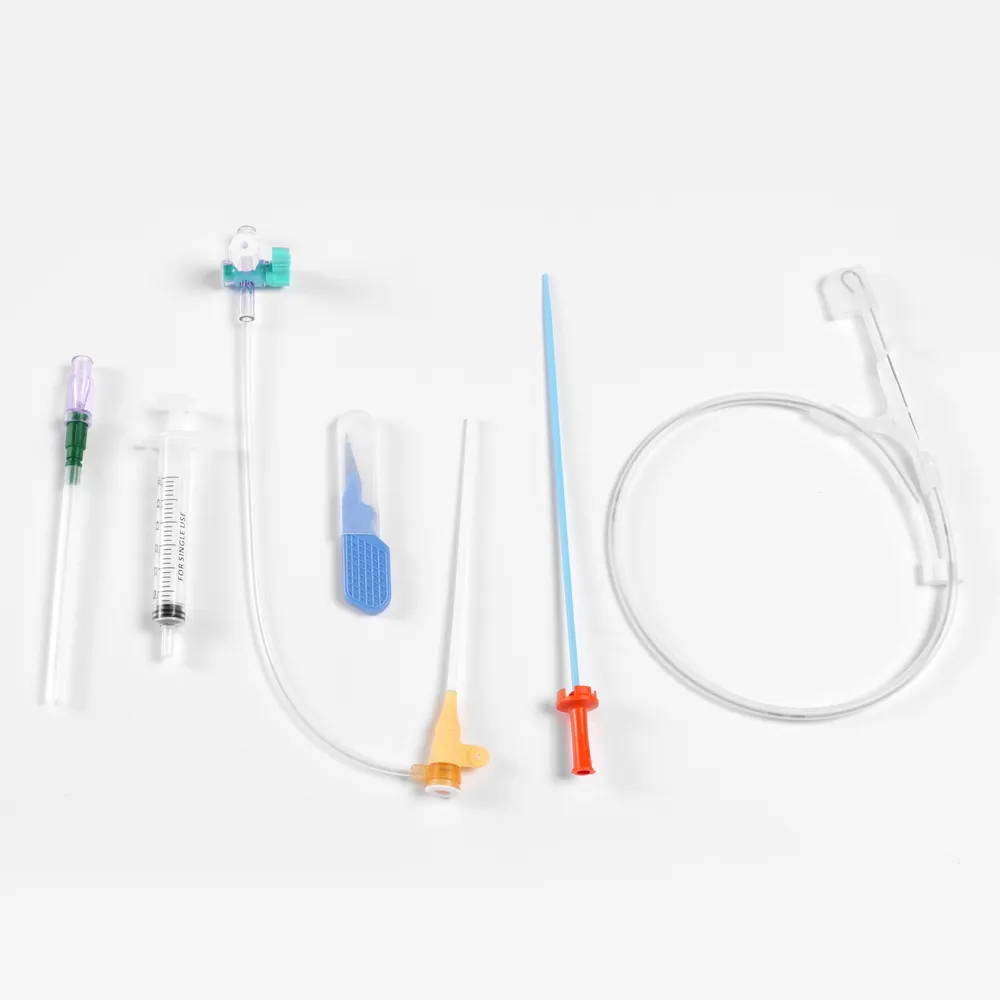 Набор интродьюсеров
Набор интродьюсеров -
 Удлинительная трубка для датчика давления
Удлинительная трубка для датчика давления -
 Гидроколлоидная повязка
Гидроколлоидная повязка -
 Набор одноразовых коаксиальный биопсийных игл
Набор одноразовых коаксиальный биопсийных игл