Транскраниальный пульсоксиметр
Если честно, когда впервые услышал про транскраниальный пульсоксиметр, мысль была простая: очередная попытка измерить невидимое. Все знают стандартный пульсоксиметр на палец — надел и видишь SpO2. А тут — череп. Скепсис был, да и коллеги в отделении неврологии сначала крутили у виска. Главный миф, который сразу надо развеять: это не рентген мозга и не УЗДГ. Аппарат не показывает тромб или очаг ишемии. Он измеряет церебральную сатурацию (rSO2) — насыщение кислородом гемоглобина в капиллярах коры головного мозга. И вот здесь начинается самое интересное, а часто — и самое сложное.
От теории к первому датчику: что обещают и что держишь в руках
В теории всё гладко. Два светодиода (чаще инфракрасный и красный), два фотодетектора, принцип спектрофотометрии — как в обычном оксиметре, но для другой ткани. На практике же первый же датчик, который мне довелось тестировать лет пять назад, вызывал больше вопросов, чем давал ответов. Крепление на голову — неудобное, особенно для пациентов в беспокойном состоянии или с особенностями анатомии. Сигнал пропадал от малейшего смещения. И главное — калибровка. В инструкции написано ?установите и начните мониторинг?. А на деле — какой базовый уровень rSO2 считать нормой для этого конкретного пациента? 60%? 70%? Производители дают широкий коридор, иногда от 55 до 75, что для клинического решения слишком расплывчато.
Именно тогда я начал понимать, что ключ — не в самом факте измерения, а в динамике. Абсолютные цифры мало о чём говорят, а вот падение на 20% от исходного уровня пациента — уже серьёзный сигнал. Это как с ЭЭГ — часто важна не абсолютная амплитуда, а её изменения. Но чтобы отслеживать динамику, нужна стабильность сигнала, которой у тех ранних моделей не было. Мы тратили кучу времени на то, чтобы просто ?поймать? устойчивую кривую.
Здесь стоит отметить, что прогресс не стоит на месте. Сейчас на рынке появляются более совершенные системы. Например, я обратил внимание на разработки компании ООО Шэньчжэнь Хуаньцю Канлянь Медикал Технологии. Их подход, судя по материалам на сайте https://www.ghlmedical.ru, близок к тому, чего не хватало раньше: интеграция искусственного интеллекта для анализа сигнала и фильтрации артефактов. Их философия ?переосмысливать здоровое будущее с помощью технологий, основанных на человеческом подходе? — это как раз про удобство и надёжность в реальных условиях, а не в идеальной лаборатории. Пока не пробовал их аппараты вживую, но спецификация выглядит продуманной.
Кардиохирургия и нейрореанимация: где он действительно нужен
Основная ниша для транскраниального оксиметра — это, конечно, интраоперационный мониторинг при операциях с высоким риском церебральной ишемии. Кардиохирургия, особенно с искусственным кровообращением — классика. Помню случай: плановая АКШ, у пациента в анамнезе транзиторные ишемические атаки. На этапе пережатия аорты rSO2 на левом полушарии начало плавно, но неуклонно снижаться, в то время как системное давление и сатурация были в норме. Анестезиолог, глядя на наш монитор, скорректировал перфузию и положение головы. Спад остановился, потом значения вернулись. После операции пациент очнулся без неврологического дефицита. Без этого датчика мы бы просто не увидели эту ?тихую? гипоперфузию.
Второе поле — нейрореанимация, ЧМТ, субарахноидальные кровоизлияния. Здесь мониторинг помогает оценивать адекватность церебрального перфузионного давления, эффективность гипервентиляции (которую, кстати, теперь применяют гораздо осторожнее). Но есть нюанс: при отёке мозга, при изменении геометрии тканей, показания могут искажаться. Нельзя слепо доверять одной цифре. Это инструмент в панели мониторинга, а не истина в последней инстанции.
А вот в отделении общей реанимации для септических пациентов его применение до сих пор спорно. Да, есть исследования о корреляции низкого rSO2 с плохим прогнозом при сепсисе. Но на практике внедрить рутинный мониторинг сложно: дорого, требует времени на установку и интерпретацию, а доказательная база для чётких протоколов действий по его показаниям ещё не так сильна, как для того же ScvO2.
Подводные камни: артефакты, анатомия и ?человеческий фактор?
Самая большая головная боль — артефакты. Движение пациента — это катастрофа для сигнала. Даже лёгкий тремор или беспокойство могут имитировать падение сатурации. Современные алгоритмы стали лучше с этим бороться, но идеала нет. Приходится постоянно визуально контролировать качество сигнала на кривой, а не просто смотреть на цифру на экране.
Анатомия — отдельная тема. Толщина кости, наличие гематомы или послеоперационного отёка под датчиком, даже густота волос — всё влияет. У одного пациента датчик лёг идеально, у другого — постоянная ?борьба? за контакт. Иногда приходится пробовать разные позиции на лбу (стандартно — над надбровной дугой), чтобы найти точку с устойчивым сигналом. Это не ?надел и забыл?, это именно мониторинг, требующий внимания.
И, конечно, человеческий фактор. Медсестра, не обученная тонкостям установки, может неплотно прикрепить датчик. Врач, не понимающий физиологии rSO2, может сделать неверные выводы. Однажды был прецедент, когда коллега начал ?поднимать? церебральную сатурацию увеличением FiO2 до 100% у пациента с нормальным PaO2, хотя проблема была в низком сердечном выбросе. Аппарат показал улучшение, но это было лишь временное изменение, не затрагивающее суть проблемы с перфузией. Обучение персонала — это 50% успеха.
Взгляд в будущее: интеграция и персонализация
Куда всё движется? Мне видится путь к интеграции. Транскраниальный пульсоксиметр не должен быть отдельным ящиком с экраном. Его данные должны в реальном времени поступать в общую систему мониторинга пациента и анализироваться вместе с ЭЭГ, ЭКГ, инвазивным давлением, температурой. Только тогда мы получим целостную картину оксигенации мозга. Некоторые продвинутые палаты пробуют это делать, но это пока штучные решения.
Второй тренд — персонализация базовой линии. Исследования накапливают данные о том, что исходный уровень rSO2 сильно варьируется в зависимости от возраста, анемии, хронических заболеваний. Алгоритмы будущего, возможно, смогут при первом подключении быстро оценить индивидуальную норму, от которой уже и отсчитывать клинически значимые отклонения. Компании вроде Хуаньцю Канлянь, позиционирующие себя как инновационное предприятие, ориентированное на мировые рынки и интеграцию ИИ, как раз могут быть драйверами в этом направлении. Их фокус на точной диагностике и цифровой экосистеме — это то, что нужно для следующего шага.
И третий момент — удешевление и упрощение технологии. Чтобы она вышла за пределы крупных федеральных центров в региональные больницы, нужны более доступные, но не менее надёжные решения. Здесь конкуренция между производителями, включая китайских, как раз на пользу клиникам.
Выводы практика: дорогой, капризный, но иногда незаменимый помощник
Итак, что в сухом остатке? Транскраниальный пульсоксиметр — это не волшебная палочка. Это специфический, довольно капризный и дорогой инструмент. Для его применения должны быть чёткие показания: кардиохирургия, определённые нейрохирургические операции, избранные случаи в нейрореанимации. Массово ?на каждого пациента в ОРИТ? его вешать бессмысленно и накладно.
Его сила — в возможности неинвазивно, в реальном времени заглянуть в метаболизм коры мозга и поймать момент, когда системные показатели ещё ?молчат?. Но его слабость — в зависимости от качества установки, интерпретации и понимания его ограничений. Это инструмент для подготовленной команды.
Лично я с осторожным оптимизмом смотрю на развитие этой технологии. Когда видишь, как на операции благодаря этому датчику удаётся предотвратить потенциальную катастрофу, понимаешь, что игра стоит свеч. Главное — не гнаться за модой, а чётко знать, зачем он тебе нужен, и уметь отличить реальный сигнал от артефакта. А это приходит только с опытом, который не купишь вместе с аппаратом.
Соответствующая продукция
Соответствующая продукция
Самые продаваемые продукты
Самые продаваемые продукты-
 Удлинительная трубка для датчика давления
Удлинительная трубка для датчика давления -
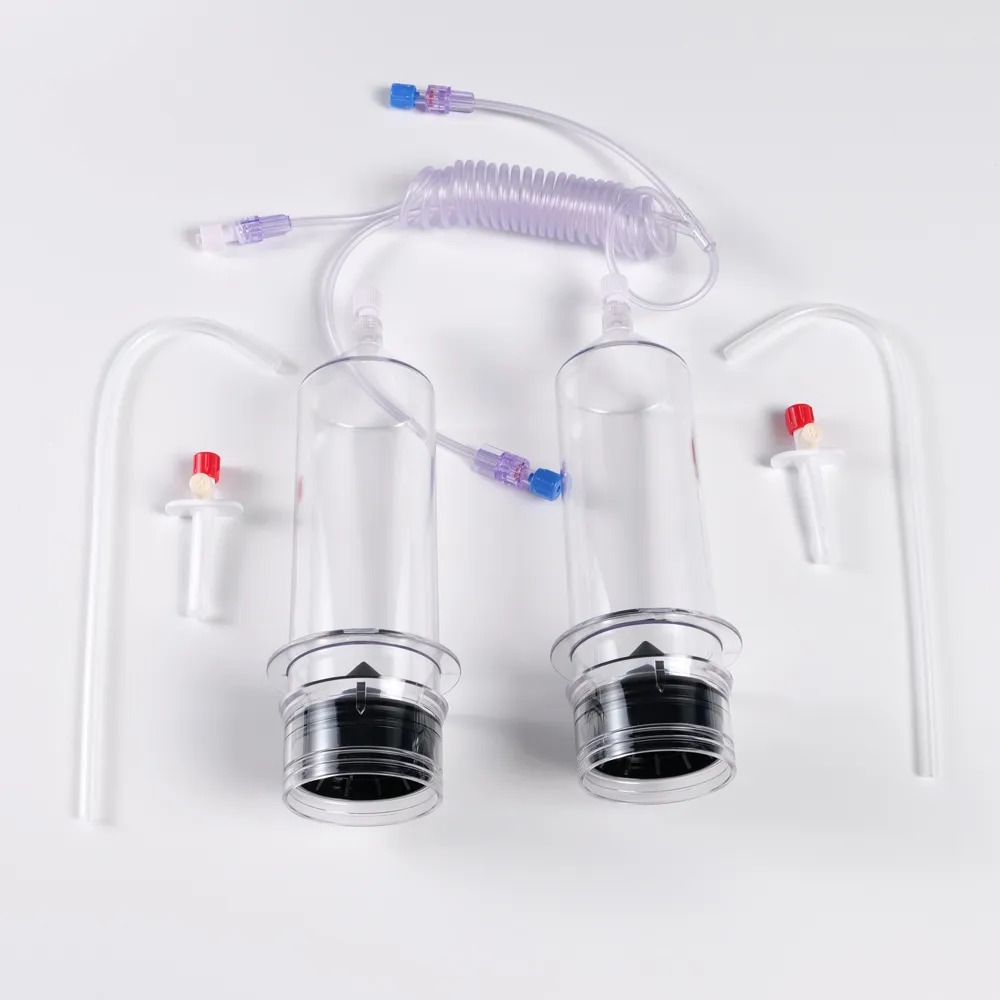 Одноразовый шприц для автоматического инъектора высокого давления, двухкамерный (для МРТ)
Одноразовый шприц для автоматического инъектора высокого давления, двухкамерный (для МРТ) -
 Нитриловые перчатки
Нитриловые перчатки -
 Одноразовый шприц для автоматического инъектора высокого давления, однокамерный (для КТ) W01
Одноразовый шприц для автоматического инъектора высокого давления, однокамерный (для КТ) W01 -
 Аптечка первой помощи для дома 3
Аптечка первой помощи для дома 3 -
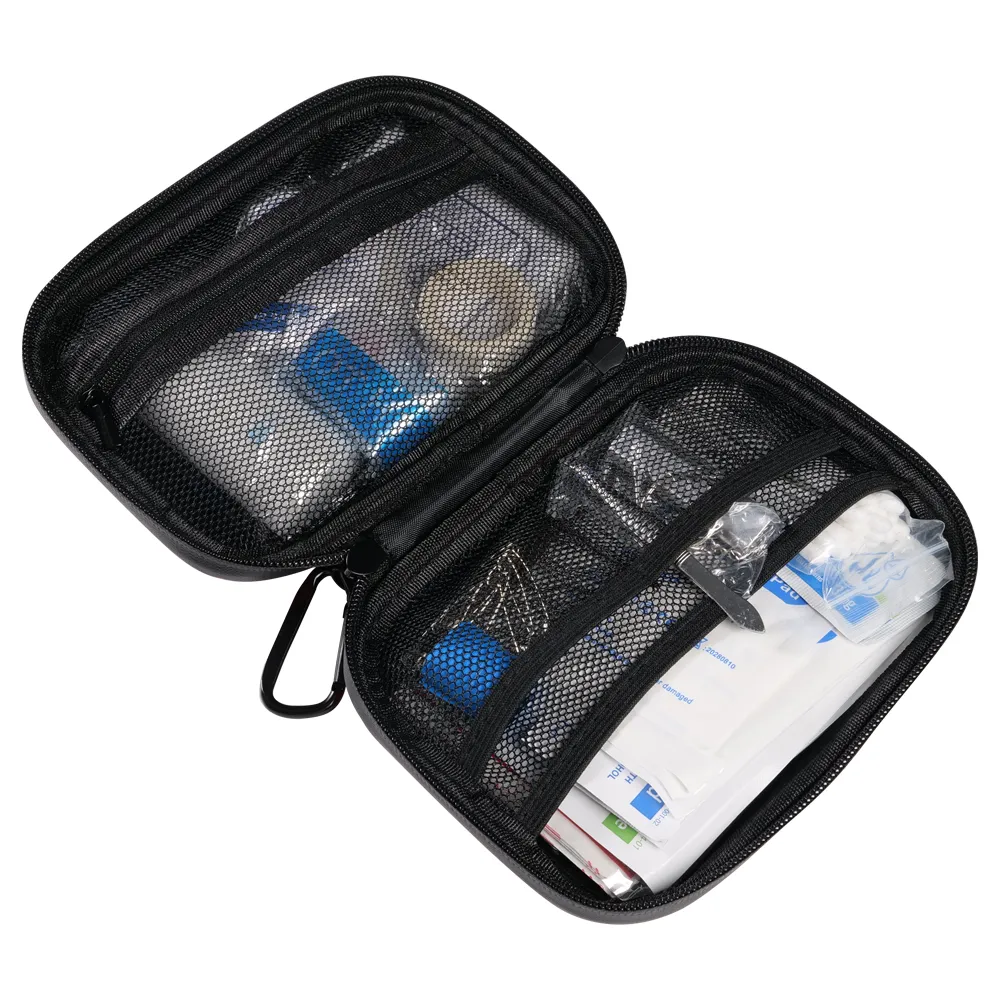 Аптечка первой помощи для дома 1
Аптечка первой помощи для дома 1 -
 Пульсоксиметр
Пульсоксиметр -
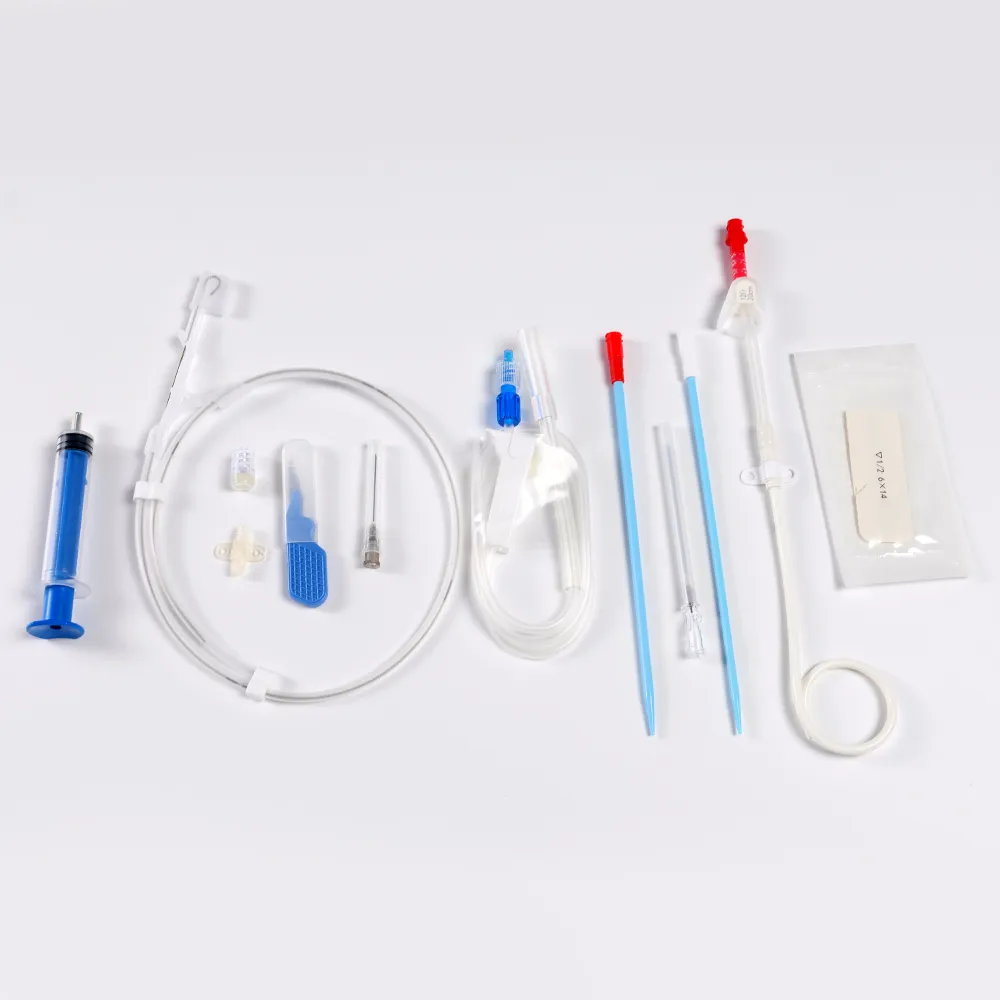 Набор для перитонеального дренажа
Набор для перитонеального дренажа -
 Одноразовый шприц для автоматического инъектора высокого давления, однокамерный (для КТ) Y01
Одноразовый шприц для автоматического инъектора высокого давления, однокамерный (для КТ) Y01 -
 Набор одноразовых коаксиальный биопсийных игл
Набор одноразовых коаксиальный биопсийных игл -
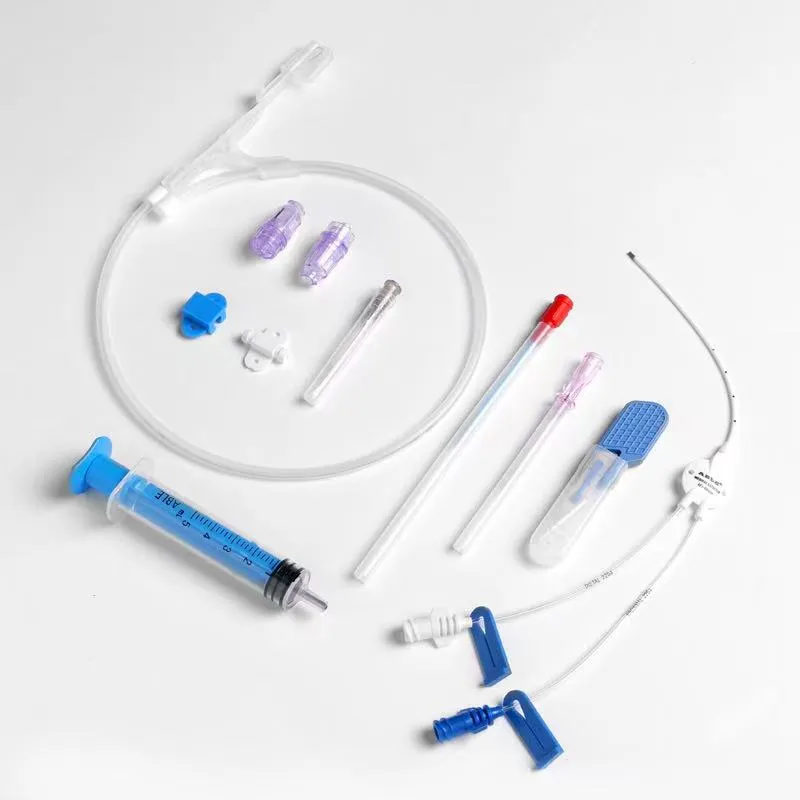 Набор для катетеризации центральной вены
Набор для катетеризации центральной вены -
 Набор дренажного катетера для однократной пункции (комплектный)
Набор дренажного катетера для однократной пункции (комплектный)
Связанный поиск
Связанный поиск- Набор для перитонеального дренажа
- Кислородная маска амбу
- Глюкометр фристайл
- Кислородная маска эффект
- Пульсоксиметр на ухо
- Одноразовый шприц для автоматического инъектора высокого давления, однокамерный (для кт)
- Самые точные пульсоксиметры
- Набор одноразовый с центральным венозным катетером
- Градусники фирмы
- Глюкометр компакт